잔글 (→구조) |
편집 요약 없음 |
||
| (다른 사용자 한 명의 중간 판 5개는 보이지 않습니다) | |||
| 1번째 줄: | 1번째 줄: | ||
{{원소정보 | |||
|이름 = 리튬 | |||
|원소기호 = Li | |||
|원자번호 = 3 | |||
|영어명 = Lithium | |||
|라틴명 = Lithium | |||
|원자량 = 6.938, 6.997g/mol | |||
|족 = 1 | |||
|주기 = 2 | |||
|원소분류 = 알칼리 금속 | |||
|발견자 = 아르프베드손(스웨덴, 1817) | |||
|실온상태 = 고체 | |||
|녹는점 = 180.5 ℃ | |||
|끓는점 = 1330 ℃ | |||
|밀도 = 0.534 g/cm³ | |||
|전기음성도 = 0.98 | |||
|존재비 = 지각 20ppm:남미 염호와 암염에 주로 존재 | |||
|산화상태 = 1 | |||
|천연 동위원소 수 = 2: 6Li(7.6%), 7Li(92.4%) | |||
|이온화 에너지 = 520.2 | |||
|원소명 어원 = [그리스어]lithos(돌) | |||
|겉보기/특성 = 은백색의 가장 가벼운 금속. 불꽃은 붉은색. | |||
|생산/합성 = 주로 리튬 함유 염수에서 분리.금속은 용융 LiCl/KCl 의 전기분해 | |||
}} | |||
[[영어]]: Lithium | [[영어]]: Lithium | ||
| 7번째 줄: | 31번째 줄: | ||
리튬은 알칼리 금속에 속하는 화학 원소이다. | 리튬은 알칼리 금속에 속하는 화학 원소이다. | ||
=원자구조= | =이름의 유래= | ||
[[파일:리튬 원자모형.png| | 돌을 뜻하는 그리스어 리토스(λίθος, líthos)에서 이름이 유래되었는데 이유는 [[나트륨]]이나 [[칼륨]]과는 달리 광석에서 처음으로 발견했기 때문이다. | ||
==설명== | |||
고성능 전지를 만드는 원소이다. | |||
==원자구조== | |||
[[파일:리튬 원자모형.png|250픽셀|섬네일|오른쪽|리튬 원자모형]] | |||
핵에 양성자 세 개를 지니고 있으며, 첫 번째 전자껍질에 전자 둘, 두 번째 전자껍질에 전자 하나를 지니고 있다. | 핵에 양성자 세 개를 지니고 있으며, 첫 번째 전자껍질에 전자 둘, 두 번째 전자껍질에 전자 하나를 지니고 있다. | ||
| 14번째 줄: | 45번째 줄: | ||
무르고 은백색이며 [[부식]]을 유발한다. [[합금]]으로 [[열전달]]이나 [[전지]] 등에 사용할 수 있으며, 미네랄 오일에는 리튬 염의 형태로 첨가되어 있는 경우가 많다. | 무르고 은백색이며 [[부식]]을 유발한다. [[합금]]으로 [[열전달]]이나 [[전지]] 등에 사용할 수 있으며, 미네랄 오일에는 리튬 염의 형태로 첨가되어 있는 경우가 많다. | ||
= | =쓰임새= | ||
배터리에 사용된다. 대부분의 휴대폰, 노트북 등 IT기기에 사용되는 배터리는 리튬으로 만들어진 리튬 이온 배터리이며, 최근 부상하는 전기차에 사용되는 배터리 또한 리튬 이온 배터리이다. | |||
=채굴량= | |||
2019년 리튬 채굴량은 7만 7,000톤인데<ref>[https://pubs.usgs.gov/periodicals/mcs2020/mcs2020-lithium.pdf U.S. Geological Survey, Mineral Commodity Summaries, January 2020]</ref>, [[오스트레일리아]] 42,000톤, [[칠레]] 18,000톤, [[중국]] 7,500톤, [[아르헨티나]] 6,400톤 순<ref>[https://pubs.usgs.gov/periodicals/mcs2020/mcs2020-lithium.pdf U.S. Geological Survey, Mineral Commodity Summaries, January 2020]</ref> 이었다. | |||
==그림== | |||
{{빈문단}} | |||
{{주기율표}} | {{주기율표}} | ||
{{분류|리튬|알칼리 금속|화학 원소}} | |||
=각주= | =각주= | ||
<references/> | <references/> | ||
2020년 12월 13일 (일) 20:48 기준 최신판
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
기본 정보 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
영어명 |
Lithium |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
라틴명 |
Lithium |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
주기율표 정보 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원자번호 |
3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원소기호 |
Li |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원자량 |
6.938, 6.997g/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
족 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
주기 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원소분류 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원소의 성질 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
실온상태 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
녹는점 |
180.5 ℃ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
끓는점 |
1330 ℃ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
밀도 |
0.534 g/cm³ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
전기음성도 |
0.98 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
산화상태 |
1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
천연 동위원소 수 |
2: 6Li(7.6%), 7Li(92.4%) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
이온화 에너지 |
520.2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
기타 정보 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
존재비 |
지각 20ppm:남미 염호와 암염에 주로 존재 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
겉보기/특성 |
은백색의 가장 가벼운 금속. 불꽃은 붉은색. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
생산/합성 |
주로 리튬 함유 염수에서 분리.금속은 용융 LiCl/KCl 의 전기분해 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원소명 어원 |
[그리스어]lithos(돌) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
발견자 |
아르프베드손(스웨덴, 1817) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
영어: Lithium
원소 기호: Li[1]
원자 번호: 3
개요
리튬은 알칼리 금속에 속하는 화학 원소이다.
이름의 유래
돌을 뜻하는 그리스어 리토스(λίθος, líthos)에서 이름이 유래되었는데 이유는 나트륨이나 칼륨과는 달리 광석에서 처음으로 발견했기 때문이다.
설명
고성능 전지를 만드는 원소이다.
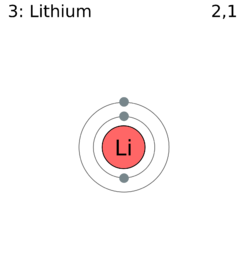
원자구조
핵에 양성자 세 개를 지니고 있으며, 첫 번째 전자껍질에 전자 둘, 두 번째 전자껍질에 전자 하나를 지니고 있다.
특징
무르고 은백색이며 부식을 유발한다. 합금으로 열전달이나 전지 등에 사용할 수 있으며, 미네랄 오일에는 리튬 염의 형태로 첨가되어 있는 경우가 많다.
쓰임새
배터리에 사용된다. 대부분의 휴대폰, 노트북 등 IT기기에 사용되는 배터리는 리튬으로 만들어진 리튬 이온 배터리이며, 최근 부상하는 전기차에 사용되는 배터리 또한 리튬 이온 배터리이다.
채굴량
2019년 리튬 채굴량은 7만 7,000톤인데[2], 오스트레일리아 42,000톤, 칠레 18,000톤, 중국 7,500톤, 아르헨티나 6,400톤 순[3] 이었다.
그림
![]() 빈문단 입니다. 내용을 추가해 주세요.
빈문단 입니다. 내용을 추가해 주세요.